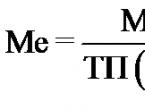A hisztidin szerkezeti képlete. A hisztidin szerkezeti kémiai képlete. A hisztidin hasznos tulajdonságai
A hisztidin vagy l hisztidin azon nem esszenciális aminosavak egyike, amely számos enzim részét képezi. Fő tulajdonsága, hogy segíti a szövetek növekedését és regenerálódását. A hisztidin a hisztamin termelése során termelődik, számos élelmiszerben megtalálható, és számos betegség, például reumás ízületi gyulladás, vérszegénység vagy fekélyek kezelésére van szükség. Jelentős koncentrációban található a hemoglobinban. Ennek az aminosavnak a hiánya súlyos következményekkel járhat.
Funkciók
A hisztidin az idegsejteket borító mielinhüvelyekben található. Fontos szerepet játszik a szervezet fertőzésekkel szembeni védelmében. Ez az aminosav nemcsak javítja az immunitást, hanem ellenáll a sugárzásnak is.
A hisztidin vagy l hisztidin a nem esszenciális aminosavak közé tartozik
Nem kevésbé fontos az a tény, hogy segít eltávolítani a nehézfémek sóit a szervezetből. A hisztamin elősegíti a belső szervek intenzívebb véráramlását. Ez növeli a szexuális vágyat is.
E fontos aminosav nélkül a szervezet védtelenné válik, és nem tud ellenállni a stressznek és a depressziónak. Az aminosav ellenáll az idegrendszer és a test egészének kedvezőtlen külső körülményeivel szemben.
A hisztidint gyakran használják gyomor- és nyombélfekély kezelésére. Csökkenti a fájdalmat, meggyógyítja az érintett szöveteket és megállítja a vérzést. A hisztidin a parenchymalis hepatitis kezelésében is hatékony.
Az aminosavat aktívan használják az immunhiányos vírus kezelésében. Hiánya köztudottan súlyos hallásproblémákhoz vezethet.

A hisztidint gyakran használják gyomorfekély kezelésére.
Hatás a testre
Mivel a hisztidin számos aktív enzim része, befolyásolja a funkciókat és az állapotot:
- máj,
- Gyomor-bélrendszer,
- Mellékvese,
- idegrendszer,
- Izom-csontrendszeri szövet.
Különleges tulajdonságai miatt ez az aminosav részt vesz a következők előállításában:
- karnozin,
- Lisztamina,
- Anzerina.

A hisztidin részt vesz a hemoglobintermelésben
Használata segít a következő betegségek kezelésében és az olyan problémák kiküszöbölésében, mint pl.
- allergiás reakciók,
- Stressz és depresszió
- Rheumatoid arthritis,
- gyomor- és nyombélfekély,
- Anémia,
- Gyomorhurut,
- Érelmeszesedés,
- Urémia,
- Májgyulladás,
- csökkent immunitás,
Olyan eljárásokban is használják, amelyek célja egy személy helyreállítása súlyos sérülések és betegségek után.

A hisztidin aminosav segít a hepatitis kezelésében
Hiány és felesleg
Egy személynek legalább 2 grammra van szüksége naponta. Ha ennek a fontos aminosavnak a mennyisége nem elegendő, vagyis lényegesen kevesebb a megállapított normánál, akkor visszafordíthatatlan változások következhetnek be a szervekben.
Az aminosav hiánya izomfájdalmat és gyulladást okozhat. Egy személy hallása károsodhat vagy teljesen elveszhet. Mindkét nemnél a szexuális vágy jelentősen csökken.
Azonban nemcsak a hisztidin hiánya lehet veszélyes. Feleslege is káros. Ha az aminosav feleslegben van jelen a szervezetben, az idegrendszeri problémákat okozhat.
Ennek feleslege elnyomhatja a neuronok aktivitását. Ennek eredményeként a személy ingerlékeny és izgatott lesz. Végső soron ez neurózishoz vezethet.
A mániás-depresszív pszichózisban szenvedők egyáltalán nem használhatnak hisztidin készítményeket. Az anyag mennyisége elegendő, amit a rendszeresen fogyasztott termékek tartalmaznak.
A hisztidinben gazdag ételeket feltétlenül be kell venni az étrendbe. Hiszen az emberi szervezet ezt az aminosavat csak részben tudja előállítani. Hiányát könnyű elkerülni, ha elegendő gabonafélét eszel. Milyen egyéb termékek tartalmazzák?
fő források
Az L hisztidin számos élelmiszerben megtalálható. A legtöbb benne van:
- lencse,
- Földimogyoró,

Az L hisztidin a földimogyoróban található
- lazac,
- tonhal,
- Szójabab.
Milyen élelmiszerek tartalmazzák ezt az aminosavat a fent felsoroltakon kívül? Elegendő mennyiségben megtalálható néhány zöldségben és gyümölcsben:
- cékla,
- uborka,
- spenót,

Az L hisztidin a spenótban található
- retek,
- fokhagyma,
- ananász,
- almák.
A vegetáriánusok számára nagyon fontos tudni, hogy milyen növényi ételek tartalmaznak hisztidint, mert nem esznek húst és halat.
A hisztidint tartalmazó élelmiszerek használata támogatja a gyomor-bél traktus munkáját. Különösen hasznos a gyomornedv savasságának csökkenésével járó rendellenességek esetén.
(béta-imidazolil-alfa-aminopropionsav, C 6 H 9 N 3 O 2) egy heterociklusos aminosav, amely túlnyomórészt bázikus tulajdonságokkal rendelkezik, szinte minden fehérjében megtalálható.
Szerkezeti képlet:
Az emberek és állatok vérében és szöveteiben, növényi szervezetekben fehérjék összetételében, valamint szabad formában és egyes származékok formájában van jelen, ch. arr. peptidek - karnozin (lásd) és anszerin (lásd). Az emberi plazma kb. 1,7 mg% G; meglehetősen nagy mennyiségben (napi 100 mg felett) a G. a vizelettel ürül (terhesség alatt nő a vér G.-tartalma és a vizelettel történő kiválasztódása). Bár a G. emberi táplálékban való jelenlétének szükségessége nem bizonyított, és nem esszenciális aminosavakként emlegetik, a patkányok, kutyák, egerek, csirkék és sok más állat étrendjében nem pótolható. A Neurospora crassa és más gombák tartalmazzák a G. betaint - hercinint és tiol származékát, az ergothioneint (lásd Betainok). Ezek a vegyületek az emberek és számos állat vérében is megtalálhatók, de nyilvánvalóan nem szintetizálódnak az állati szervezetben, és táplálékkal kerülnek be.

A G.-t először A. Kossel állította elő 1896-ban a tokhal protamin hidrolizátumából - sturinból, és ugyanebben az évben S. Hedin - a kazein hidrolizátumából. A G. más fehérjék hidrolizátumaiból is előállítható. Sok G. tartalmaz globint (a hemoglobin fehérje részét), aminek köszönhetően a vér gazdag forrása a G.-nek.
A G. színtelen lemezek formájában kristályosodik, vízben jól fogunk oldódni, rossz - alkoholban, éterben és kloroformban nem oldódik, t ° pl 277 ° (bomlással). G. izoelektromos pontja pH 7,6. A természetes L-hisztidin, [a] 20 D -39,3, enyhén keserű ízű.
A hisztidin, mint gyógyszer
Histidinum hisztidin-hidroklorid formájában kapható (Histidini hydrochloridum; szinonimája: Cloristin, Gerulcin, Herulcin, Histifan, Laristin, Laristidin, Stellidin, Ulcostidin). Vízben jól feloldjuk. Bármilyen beadási mód esetén gyorsan felszívódik.
G. enyhén fokozza a szekréciós és motoros funkciót ment.- kish. egy olyan út, amely valószínűleg egy hisztamin G.-ből származó oktatáshoz kapcsolódik. G. feltárja az adaptogén tulajdonságait: a táplálékban található nagy mennyiségben csökkenti a magas hőmérséklet, az alacsony légköri nyomás és az ionizáló sugárzás negatív hatását az állatokra; ugyanakkor a G metabolizmusában részt vevő enzimek aktivitása.
Alkalmazza a G.-t hepatitis, hron, magas savasságú gastritis, gyomor- és nyombélfekély kezelésére. Adja be intramuszkulárisan 5 ml 4% -os oldatban naponta. A kezelés időtartama 20-30 injekció, majd 2-3 havonta 5-6 injekciót írnak elő. G. javítja az egészséget, az alvást, megszünteti a fájdalmat és a diszpepsziát; a betegek jelentős részében a gyomornyálkahártya regenerációja vagy a fekély hegesedése figyelhető meg. Parenchymalis hepatitis esetén a hasonló kezelés felgyorsítja a gyógyulást, gyorsabban normalizálja a máj pigment-, protrombinképző és szintetikus funkcióit. A G. komplex antireumatikus kezelésben használatos. Az érelmeszesedésben szenvedő betegeknél a G. javítja a lipidanyagcserét. G. készítményeinek általában nincs mellékhatása. Időnként gyorsan múló gyengeség, sápadtság, fájdalom jelentkezik az epigasztrikus régióban.
Kiadási űrlap: 5 ml-es ampullák 4% -os oldattal; fénytől védett helyen tároljuk.
Bibliográfia Braunstein A. E. Biochemistry of aminosav metabolizmus, M., 1949, bibliogr.; Vizir A. D. A hisztidin alkalmazása atherosclerosisban, Vrach, eset, 7. sz. 129, 1964; Meister A. Az aminosavak biokémiája, transz. angolból, M., 1961; Mardashev G. R. Az orvostudomány biokémiai problémái, p. 109, Moszkva, 1975; Shelygina H. M. A hisztidin hatása a vaszkuláris permeabilitásra reumában, Kazansk. édesem. folyóirat, 4. sz. 19, 1968; A qui st H. P. a. Tg u p i n J. S. Aminosav metabolizmus, Ann. Fordulat. Biochem., v. 35. o. 231, 1966, bibliogr.; Hisztidin, Meth. Enzymol., v. 17B. 1. o. 1, N. Y. - L., 1971; Meister A. Az aminosavak biokémiája, v. 1-2, N. Y. - L., 1965; Truff a-Bachi P. a. Cohen, G. N. Aminosav metabolizmus, Ann. Bev. Biochem., v. 42. o. 113, 1973, bibliogr.
I. B. Zbareky; I. V. Komissarov (farm.).
Életünk során legalább egyszer mindannyian elgondolkodtunk az étrendünkön. Például mennyi a szervezet számára szükséges különféle anyagok napi normája, amelyek élelmiszerrel jutnak hozzánk? Milyen aminosavakra van szükségünk és miért? Ma persze nem fogunk általánosságban beszélni a helyes táplálkozásról, hiszen ehhez egy vagy akár egy tucat cikk sem elég. Csak egy anyagról beszéljünk, amely kétségtelenül nagyon fontos a szervezet számára. hisztidin. A kémiai neve bonyolultan hangzik – L-2-amino-3-(1H-imidazol-4-il) De először is.
Mi az aminosav?
Mielőtt a hisztidin tulajdonságairól és a szervezetben betöltött szerepéről beszélnénk, foglalkozzunk az „aminosav” fogalmával. Azok, akik szerették a sportot, hallottak ezekről az anyagokról. Az aminosav olyan szerves vegyület, amelynek két fő funkciós csoportja teszi különlegessé: az aminocsoport -NH 2 és az úgynevezett -COOH karboxilcsoport.
Az első a vegyület e szokatlan osztályának fő tulajdonságaiért felelős. A nitrogénnek és elektronpárjának köszönhetően egy aminosav pozitív töltésű ionokat képezhet. Ebben az esetben az aminocsoport ilyen ionná alakul: -NH 3 +.
A második funkcionális csoport felelős a Képes protont adományozni, anionná alakulva -COO -. Ez a jelenség lehetővé teszi sók képzését a karboxilcsoport oldaláról.
Így egy aminosavnak két része van, amelyek mindegyike képes sókat képezni. Egyikük ezeket a vegyületeket savakkal, a másik pedig bázisokkal biztosítja. Általában egy aminosav a következőképpen ábrázolható: NH2-CH(R)-COOH. Az R betűt itt "gyökként" kell érteni, vagyis minden olyan szerves részecskét, amely funkcionális csoportokból és szénvázból áll, és képes kötést (vagy kötéseket) kialakítani egy aminosavmolekula gerincével.
Általában még azok is, akik nem járatosak a farmakológiában és nem szerettek sportolni, legalább egyszer hallották, legalábbis a reklámokból, hogy szükségünk van az aminosavakra, és nagyon hasznosak. Nézzük meg, milyen funkciókat látnak el a szervezetben, és miért kell az élelmiszerből a szükséges normát bevinni.
szervezetben
Mint tudod, mindannyian fehérjékből, zsírokból és szénhidrátokból állunk. Élelmiszerként fogyasztjuk őket életképességünk megőrzése érdekében. A cikk témájában azonban csak a fehérjék érdekelnek minket. Hatalmas molekulákról van szó, amelyek egészen más és nagyon fontos funkciókat látnak el szervezetünkben: anyagok szállítását, új sejtek létrehozását, valamint az agyi neuronok közötti kapcsolatok erősítését.

Okkal kezdtünk beszélni a fehérjékről. Az a tény, hogy minden ilyen anyag aminosavakból áll, amelyek magukban foglalják a hisztidint. Még a legegyszerűbb fehérje képletében is legalább egy tucat aminosav kapcsolódik egy polipeptidláncba. Mindegyiknek megvan a maga szerkezete és alakja, amely lehetővé teszi, hogy ellátja azt a funkciót, amelyre a természet létrehozta.
hisztidin
Bármely aminosav képlete, amint azt már megtudtuk, legalább két funkciós csoportot és egy ezeket összekötő szénvázat tartalmaz. Éppen ezért a különbség az összes aminosav között (amelyből egyébként már több milliót találtak) a két csoport közötti szénhíd hosszában és a hozzá kapcsolódó gyök szerkezetében rejlik.

Cikkünk témája az egyik aminosav - hisztidin. Ennek az esszenciális savnak a képlete nem egyszerű. A két funkciós csoport közötti fő szénláncban csak egy szénatomot látunk. Valójában az összes esszenciális proteinogén (fehérjék előállítására képes) aminosavnak is csak egy szénatomja van ebben a láncban. Ezenkívül a hisztidin komplex gyökszerkezettel rendelkezik, amely ciklust is tartalmaz. Fent láthatja, mi az a hisztidin. amelynek sajátossága a heterociklusban rejlik (a szénen kívül minden más atom befogadása), valójában messze nem a legösszetettebb anyag.
Tehát, mivel az alapfogalmakat elemeztük, térjünk át a hisztidinnel végrehajtható reakciókra.
Kémiai tulajdonságok
A reakciók, amelyekbe ez az aminosav belép, nagyon kevés. A savakkal és bázisokkal való reakciók mellett biuret reakcióba lép, és színes termékeket képez. Ezenkívül a hisztidin, amelynek képlete imidazol-maradékokat tartalmaz, kölcsönhatásba léphet a szulfanilsavval a Pauli-reakció során.

Következtetés
Az összes fő részletet ismertettük. Reméljük, hogy a cikk hasznos volt az Ön számára, és új ismereteket adott.
A szervezetben a dekarboxiláció során hisztaminná alakul át
A hisztidin (rövidítve His vagy H) egy imidazol funkciós csoportot tartalmazó alfa-aminosav. Ez egyike a 22 proteinogén aminosavnak. A CAU és CAC kodonok jelölik. A hisztidint Kossel Albrecht német orvos fedezte fel 1896-ban. A hisztidin nélkülözhetetlen az emberek és más emlősök számára. Kezdetben úgy gondolták, hogy ez csak a csecsemők számára nélkülözhetetlen, de a hosszú távú vizsgálatok során kiderült, hogy ez a felnőttek számára is fontos.
Kémiai tulajdonságok
A hisztidin imidazol oldalláncának pKa értéke (a disszociációs állandó negatív decimális logaritmusa) körülbelül 6,0, és általában pKa értéke 6,5. Ez azt jelenti, hogy fiziológiailag megfelelő pH-értékeknél a pH viszonylag kis változása megváltoztathatja az átlagos lánctöltést. pH 6 alatt az imidazolgyűrű többnyire protonált, mint a Henderson-Hasselblach egyenletben. Protonálva az imidazolgyűrű két NH-kötéssel és pozitív töltéssel rendelkezik. A pozitív töltés egyenletesen oszlik el a két nitrogénatom között.
Aroma
A hisztidin imidazolgyűrűje minden pH-értéken aromás. Hat pi elektront tartalmaz: négyet két kettős kötésből és kettőt egy nitrogénpárból. Képes pi-kötéseket kialakítani, de ezt nehezíti a pozitív töltése. 280 nm-en nem nyel el, de az alsó UV tartományban még egyeseknél is többet.
Biokémia
A hisztidin imidazol oldallánca a metalloproteinek közös koordináló liganduma, és bizonyos enzimek katalitikus helyeinek része. A katalitikus triádokban a bázikus hisztidin-nitrogénből protont állítanak elő, treoninból vagy -ból, és nukleofilként aktiválják. A hisztidint a protonok gyors átvitelére használják úgy, hogy a protont a bázikus nitrogénnel elvonják, és pozitív töltésű intermediereket hoznak létre, majd egy másik molekula, puffer segítségével vonják ki a protont a salétromsavból. A karboanhidrázban egy hisztidin protontranszfert használnak a protonok gyors szállítására a cinkhez kötött vízmolekulából, hogy gyorsan regenerálják az enzim aktív formáit. A hisztidin a hemoglobin E és F hélixeiben is jelen van. A hisztidin segít stabilizálni az oxihemoglobint és destabilizálni a CO-hoz kötött hemoglobint. Ennek eredményeként a szén-monoxid-kötés csak 200-szor erősebb a hemoglobinban, szemben a szabad hem 20 000-szeresével.
Némelyik átváltható intermedierré a Krebs-ciklusban. Az aminosavak négy csoportjából származó szénatomok ciklus közbenső termékeket képeznek - alfa-ketoglutarát (alfa-CT), szukcinil-CoA, fumarát és oxálacetát. , alfa-KG-t képezve – glutamátot, glutamint, prolint és hisztidint. A hisztidin formiminoglutamáttá alakul (FIGLU). A formimino-csoport tetrahidrofolátra kerül, és a maradék öt szénatom glutamátot képez. A glutamát glutamát-dehidrogenázzal dezaminálható, vagy transzamináción mehet keresztül alfa-KG képzésére.
NMR (nukleáris mágneses rezonancia)
Ahogy az várható volt, ezeknek a nitrogénatomoknak a 15N kémiai eltolódása megkülönböztethetetlen (körülbelül 200 ppm a salétromsavhoz képest a szigma skálán, ahol a szűrés növekedése a kémiai eltolódás növekedésének felel meg). Ahogy a pH körülbelül 8-ra emelkedik, az imidazolgyűrű protonálódása elveszik. A most semleges imidazol maradék protonja nitrogénként létezhet, és H-1 vagy H-3 tautomereket eredményez. Az NMR azt mutatja, hogy az N-1 kémiai eltolódás enyhén, míg az N-3 kémiai eltolódás jelentősen csökken (körülbelül 190 vs. 145 ppm). Ez azt jelenti, hogy az N-1-H tautomer előnyösebb, mivel a szomszédos ammóniummal hidrogénkötések képződnek. Az N-3 védelmet jelentősen csökkenti a másodrendű paramágneses hatás, amely szimmetrikus kölcsönhatást foglal magában a nitrogén magányos pár és az aromás gyűrű gerjesztett pi* állapotai között. Ahogy a pH 9 fölé emelkedik, az N-1 és N-3 kémiai eltolódása körülbelül 185 és 170 ppm lesz. Érdemes megjegyezni, hogy az imidazol deprotonált formája, az imidazolát ion csak 14 feletti pH-értéken képződik, ezért fiziológiailag nem jelentős. Ez a kémiai eltolódás változása az ammóniumionon lévő amin-hidrogénkötés látszólagos csökkenésével, valamint a karboxilát és az NH közötti kedvező hidrogénkötéssel magyarázható. Ez arra szolgál, hogy csökkentse az N-1-H tautomer preferenciáját.
Anyagcsere
A hisztamin és a karnozin bioszintézisének előfutára.
A hisztidin ammónia-liáz enzim a hisztidint ammóniává és urokánsavvá alakítja. Ez az enzim hiányos a ritka anyagcserezavarban, a hisztidinémiában. Antinobaktériumokban és fonalas gombákban, mint például a Neurospora crassa, a hisztidin antioxidáns ergothioneinné alakulhat át.
Hisztidin az élelmiszerekben
A hisztidin olyan élelmiszerekben gazdag, mint a tonhal, lazac, sertés szűzpecsenye, marhafilé, csirkemell, szójabab, földimogyoró, lencse.
Hisztidin-kiegészítők
A hisztidin-kiegészítésről kimutatták, hogy patkányokban a cink gyors felszabadulását okozza, a kiválasztási sebesség 3-6-szoros növekedésével.